Заболеваемость
Злокачественная мезотелиома плевры (ЗМП) ― редкая опухоль. Заболеваемость составляет 1,25 на 100 тысяч в Великобритании и 1,1 на 100 тысяч в Германии. Предполагается, что в большинстве стран в течение последующих 20 лет заболеваемость удвоится. Экспозиция к асбесту является установленным этиологическим фактором в развитии ЗМП, 70-80% всех случаев ЗМП являются следствием профессиональной экспозиции к асбесту.
Диагноз
Обычно пациенты отмечают появление одышки, вследствие накопления плеврального выпота или болей в грудной клетке при запущенных стадиях. Диагноз подтверждается при помощи дополнительных рентгенологических методов исследования (одностороннее опухолевое поражение плевры, плевральный выпот). Должен быть собран и профессиональный анамнез.
С диагностической целью может быть проведено цитологическое исследование выпота, но очень часто результаты этих исследований сомнительны. Поэтому «золотым» стандартом является гистологическое исследование, включая иммуногистохимическое исследование.
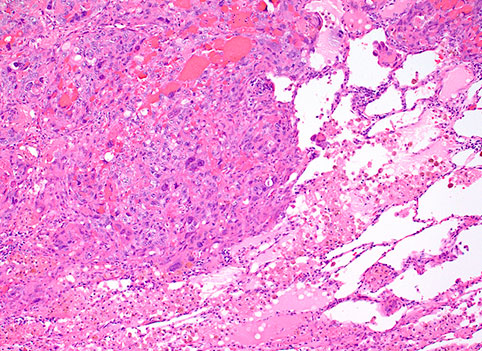
Плевроскопия, видеоассистированная торакоскопия или открытая биопсия плевры, после удаления плеврального выпота, могут быть необходимой процедурой для получения достаточного материала, с целью точного гистологического диагноза. Существует три основных гистологических типа (эпителиальный, саркоматоидный и смешанный), при этом на долю эпителиального типа приходится около 60 % всех мезотелиом.
Данные указывают на возможное использование мезотелин-подобных белков сыворотки крови и остеопонтина как маркеров при диагностировании мезотелиомы, однако их роль в качестве маркеров должна быть еще подтверждена.
Стадирование и прогноз
Клиническое стадирование проводится с помощью КТ-исследования грудной клетки. Однако стадировние по системе TNM, основанное на данных КТ, не является окончательным.
Медиастиноскопия и видео-ассистированная торакоскопия могут быть полезны для определения стадии заболевания.
Точное первичное стадирование ― основа, обеспечивающая прогностическую информацию, и руководство для выбора наиболее подходящей лечебной тактики. Существует несколько отличающихся систем стадирования. Международная система стадирования ЗМП (IMIG) придает особое значение степени распространения болезни в рамках традиционной системы TNM и стратификации больных по схожим прогностическим категориям (таблица №1).
Могут быть использованы прогностические критерии, разработанные Европейской организацией по изучению и лечению рака (EORTC). К ним относятся: общее состояние, пол, возраст, достоверность гистологического заключения, гистологический тип и число лейкоцитов.
ЗМП редко метастазирует в отдаленные органы, но основная группа пациентов поступает с далеко зашедшей местно-распространенной формой заболевания. Использование позитронно-эмиссионной томографии (ПЭТ), для исключения экстраторакальных метастазов у пациентов, с предполагаемым радикальным лечением, продолжает изучаться и является перспективным методом обследования.
Лечение
Хирургическое лечение
Разнообразные хирургические вмешательства применялись с различным успехом. Экстраплевральная пневмонэктомия (ЭПП) с резекцией половины диафрагмы и перикарда единым блоком обеспечивает возможность радикального удаления опухоли и данный подход, как правило, применяется в комбинации с химиотерапией или радиотерапией. Хирургическое лечение, правомерность которого все еще исследуется, может выполняться только у отдельных больных опытными торакальными хирургами, работающими в мультидисциплинарной команде [III,А].
Критериями отбора для ЭПП являются: удовлетворительное состояние пациента по ECOG, ранняя стадия заболевания при не более чем незначительном вовлечении передней грудной стенки и при адекватной функции легких и сердца. Данные по проведению ЭПП у больных с N2 или саркоматоидным вариантом болезни противоречивы.
Плевроэктомия/декортикация может быть показана больным с ранней стадией или при макроскопически определяемой опухоли, оставленной после ЭПП.
К паллиативным местным оперативным вмешательствам относятся париетальная плевроэктомия, или плевродез, которые выполняются для уменьшения одышки и болевого синдрома.
Таблица №1. Стадирование больных
Стадия IA T1аN0M0 Первичная опухоль ограничена ипсилатеральной париетальной плеврой
Стадия IB T1bN0M0 Также как при стадии IA плюс локальное вовлечение висцеральной плевры
Стадия II T2N0M0 Также как при стадии IA или IB плюс сливающееся вовлечение диафрагмы или висцеральной плевры или вовлечение легкого
Стадия III T3 N любое M0, Местно распространенная, потенциально резектабельная опухоль.
Стадия III T любое N1 M0, Вовлечение ипсилатеральных, бронхопульмональных лимфоузлов, лимфоузлов корня легкого.
Стадия III T любое N2 M0, Вовлечение трахеобронхиальных и ипсилатеральных медиастинальных лимфоузлов
Стадия IV T4 N любое M0, Местно распространенная, технически нерезектабельная опухоль.
Стадия IV T любое N3 M0, Вовлечение контралатеральных медиастинальных, внутренних маммарных и ипсилатеральных или контралатеральных надключичных лимфоузлов.
Стадия IV T любое N любое M1 Отдаленные метастазы
Использование конвенциальной радиотерапии с лечебной целью ограничено по причине сложности облучения, так как большой объем облучаемых тканей высокими дозами невозможен без превышения толерантности прилежащих тканей, особенно (гомолатерального) легкого.
Истинная роль лучевой терапии при мультидисциплинарном подходе в лечении ЗМП в настоящее время исследуется. Тем не менее, применение 3D конформного облучения и лучевой терапии с модулированием интенсивности (IMRT), позволяет подвести дозы облучения более 45 Гр, в попытке улучшения местного контроля после ЭПП. Однако необходимо соблюдать осторожность в отношении облучения контралатерального легкого низкими дозами радиации, особенно при применении IMRT [III, B]. Конвенциональная доза может быть подведена местно с паллиативной целью для контроля болевого синдрома [IV, C].
Мезотелиома распространяется по каналу, образующемуся при торакоскопической манипуляции, применение профилактической радиотерапии на канал введения (PIT) позволяет снижать частоту возникновения метастазов в области пункций. В отсутствии недвусмысленных проспективных исследований ― результаты рандомизированных исследований с небольшим числом больных, с различными гистологическими вариантами и различными техниками лучевого облучения ― становится невозможно дать определенное заключение по эффективности данного метода лечения [II, C].
Химиотерапия
Производные платины, доксорубицин и некоторые антиметаболиты (метотрексат, ралтитрексед, пеметрексед), применяемые в монорежимах, показали умеренную терапевтическую активность [III,В].
В рандомизированном исследовании как комбинация пеметрекседа с цисплатином, так и менее распространенная комбинация ралтитрекседа с цисплатином улучшили выживаемость, функцию легких и качество жизни, по сравнению с применением цисплатина в монорежиме [II,А]. Другой эффективной комбинацией является схема пеметрексед/карбоплатин [III,А].
Исследование III фазы по изучению эффективности 2-й линии терапии ралтитрекседом в сравнении с наилучшим симптоматическим лечением, у больных, которые ранее не получали данный препарат, продемонстрировало улучшение времени до прогрессирования в группе больных, получавших ралтитрексед.
Так как винорельбин или гемцитабин обладают активностью в монорежиме и в первой линии терапии, они могут быть рациональным выбором и при второй линии. В одном исследовании, 63 пациента получили терапию винорельбином, что позволило достичь 16% объективного эффекта, а медиана продолжительности жизни составила 9,6 месяцев [III, A].
Если планируется выполнение ЭПП, следует обсуждать назначение цисплатин- содержащей предоперационной и адъювантной химиотерапии.
Оценка эффекта лечения
Рекомендуется проводить оценку эффективности лечения с помощью КТ после 2-3 курсов химиотерапии, для оценки следует применять модифицированные RECIST критерии. Измерение объема опухоли находится на этапе исследования.
Наблюдение
Наблюдение состоит из клинической оценки, с особым вниманием к проявлению симптомов болезни или появлению рецидива в грудной стенке, и при необходимости, выполнения КТ-исследования органов грудной клетки.






