 Заболеваемость
Заболеваемость
В Европе заболеваемость взрослых острыми миелобластными лейкозами (ОМЛ) составляет 5-8/100 тыс. случаев и миелодисплатическими синдромами (МДС) 4-5 случаев на 100 тыс. в год. В возрастной группе старше 60 лет заболеваемость ОМЛ и МДС существенно возрастает, составляя уже 40-60 вновь диагностированных случаев МДС на 100 тыс. населения в год. Смертность от ОМЛ составляет 4-6 случаев на 100 тыс. ежегодно.
Диагноз
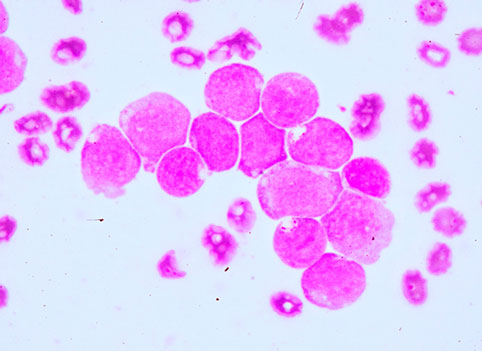
Диагноз ОМЛ и МДС базируется на основании исследования образцов периферической крови (ПК) и костного мозга (КМ). Анализ должен включать морфологическое, цитохимическое, иммунофенотипическое (более важное для ОМЛ, чем для МДС), цитогенетическое и молекулярное исследования.
Исторически подразделяемые на варианты в соответствии с описательной Франко-Американо- Британской (FAB) классификацией ОМС и МДС, в настоящее время классифицируется на основании критериев, приведенных в классификации ВОЗ, впервые изданной в 2001 году и переработанной в 2008.
Современный единый диагностический алгоритм, разработанный для ОМЛ и МДС, помимо морфологии включает данные генетики, иммунофенотипа и клиническую информацию, необходимые для выделения подтипов с разным клиническим течением. Термин «миелоидный» в классификации ВОЗ относится ко всем клеткам, принадлежащим к гранулоцитарному, гранулоцитарно/ макрофагальному и эритроидному росткам. Разделение на ОМЛ и МДС осуществляется в соответствии с процентом бластных клеток: процент, превышающий 20% в ПК или КМ, будет свидетельствовать в пользу диагноза ОМЛ, появившегося либо de novo, либо вследствие прогрессии предсуществовавшего МДС.
Бластные клетки считаются таковыми в соответствии с критериями, недавно приведенными Международной Рабочей Группы по морфологии МДС (Working Group on Morphology of MDS). В отличие от ОМЛ МДС может представлять собой диагностическую сложность, особенно в случаях с нормальным процентом бластных клеток и неоднозначной морфологической картиной.
К “минимальным” диагностическим критериям МДС относятся наличие соответствующих клинических симптомов, отчетливая дисплазия . 10% клеток миелоидного ростка в КМ, при этом должно быть исключено воздействие агентов провоцирующих вторичную дисплазию. При отсутствии четких морфологических признаков дисплазии, диагноз МДС может быть установлен только на основании обнаружения одной из характерных цитогенетических аномалий.
Диагноз МДС не может быть установлен на основании исследования иммунофенотипа методом проточной цитофлоуриметрии, при отсутствии характерных морфологических или цитогенетических признаков. В некоторых случаях рекомендуется наблюдение с регулярным повторяющимся исследованием морфологии и кариотипа в течении как минимум нескольких месяцев.
Пациенты потенциально подходящие для проведения аллогенной трансплантации (АллоТСК) и их родственники первого порядка (при наличии) должны быть HLA типированы уже во время постановки диагноза. В случаях ОМЛ высокого риска (при наличии неблагоприятных аномалий кариотипа), всегда подразумевается АллоТСК, как метод лечения, поэтому поиск совместимых неродственных доноров должен быть начат как можно раньше.
Факторы риска и прогноза
Возраст, исходное количество лейкоцитов и наличие сопутствующей патологии являются важными факторами риска при ОМЛ, в то время как прогноз зависит главным образом от принадлежности болезни к определенному подтипу.
Морфологические характеристики сохраняют свое значение для классификации МДС и выделения таких категорий как рефрактерная анемия с или без наличия кольцевидных сидеробластов или рефрактерная цитопения с мультилинейной дисплазией. Вторичный по отношению к МДС ОМЛ, обладает наихудшим прогнозом.
Лечение
При любой возможности, лечение лейкозов должно проводиться в рамках протоколов клинических исследований, в центрах с достаточным опытом соответствующего лечения, при наличии мультидисциплинарной структуры и достаточном количестве случаев. Во всех случаях ОМЛ основной целью терапии служит излечение, в то время как при МДС такая задача, к сожалению, является невыполнимой. Единственным методом излечения при МДС может быть АллоТСК, в то время как при ОМЛ достаточное количество пациентов может быть излечено без применения АллоТСК.
Интенсивная терапия пациентов с ОМЛ и некоторых пациентов с МДС, подходящих для активного лечения, подразделяется на фазу индукции, консолидации и поддерживающего лечения (редко). Потенциальные кандидаты для АллоТСК должны быть определены как можно раньше ― на этапе диагноза или индукционной терапии.
Терапия может быть начата только после (если это представляется возможным) накопления достаточного количества диагностического материала. Пациентам с высокими цифрами лейкоцитоза перед началом лечения в качестве экстренной меры может быть проведен лейкоферез.
Терапия индукции включает комбинацию антрациклинов и цитозина арабинозида, «3+7» представляет собой наиболее часто применяемый режим. Терапия индукции ОПЛ включает производное ретиноевой кислоты (all-trans retinoic acid, ATRA), являющееся стимулятором клеточной дифференцировки в комбинации с антрациклинами, при этом роль цитазаина-арабинозина до конца не ясна и необходимость его включения в схему остается спорным вопросом. Пациентам с ОПЛ должен обязательно проводиться мониторинг коагулограммы с целью своевременного выявления лейкоз- ассоциированной коагулопатии.
Применение колониестимулирующих гемопоэтических факторов во время проведения терапии индукции и их роль в сенсибилизации лейкозных клеток к химиотерапии требует уточнения. Терапия консолидации проводится после констатации клинико-гематологической ремиссии. Единый оптимальный режим терапии консолидации к настоящему моменту еще не утвержден. Пациентам, которым проведение АллоТСК не представляется возможным, рекомендуется проведение терапии консолидации высокими дозами цитарабина. В группе хорошего прогноза, где риск рецидива не превышает 35%, проведение АллоТСК в первой ремиссии не является оправданным, поскольку показатели токсичности и смертности, ассоциированные с трансплантацией, превышают показатели эффективности метода для этих пациентов.
Пациенты с ОМЛ, относящиеся к группе промежуточного и плохого прогноза, также как и МДС плохого прогноза, при наличии HLA- совместимых сиблингов при отсутствии противопоказаний являются кандидатами для проведения АллоТСК. При отсутствии совместимых сиблингов должен быть активирован поиск HLA- совместимого неродственного донора в международном регистре.
Гаплоидентичная трансплантация может рассматриваться в случае несовместимости по killer-immunoglobulin-like receptor (KIR).
Режимы кондиционирования сниженной интенсивности могу быть применены у пациентов самой старшей возрастной группы (> 50 лет). Инфекционные осложнения, появившиеся во время проведения терапии индукции должны контролироваться должным образом перед проведением АллоТСК. До сих пор остается не ясной роль высокодозной химиотерапии с реинфузией аутологичных стволовых клеток. Применение метода увеличивает время до прогрессирования и продолжительность ремиссии, однако влияние на показатели общей выживаемости остается неясным.
Терапия поддержки в настоящее время используется только для ОПЛ в первой ремиссии, при котором полностью оправдано длительное проведение химиотерапии и ATRA.
При отсутствии ответа на 1-2 курса терапии индукции болезнь признается рефрактерной, и такие пациенты имеют очень высокий риск окончательной неудачи лечения. Тщательно отобранным пациентам, при наличии HLAсовместимых доноров, может быть проведена АллоТСК, однако смертность, ассоциированная с процедурой должна всегда противопоставляться низкому шансу на успех в данной группе.
Пациентам не походящим для проведения АллоТСК, могут быть предложены системная паллиативная терапия или BSC, не обладающие, как минимум, выраженной токсичностью. Прогноз в этой группе всегда плохой, вне зависимости от интенсивности проводимой терапии.
Пациентам в рецидиве после первой ремиссии может быть проведена интенсивная терапия реиндукции, при этом шансы на успех выше у пациентов с более длительной продолжительностью первой ремиссии. Пациентам с рецидивом после второй и последующих ремиссий при наличии HLA- совместимого донора может быть проведена АллоТСК.
При рецидиве ОПЛ может быть применен триоксид мышьяка, который способен вызывать ремиссии даже в случаях вторичной рефрактерности к АТRА. Требует уточнения эффективность триоксид мышьяка в качестве терапии первой линии при ОПЛ.
Оценка эффективности лечения и наблюдение
Эффективность терапии МДС и ОМЛ клинически оценивается при помощи рутинного анализа периферической крови с подсчетом формулы и исследования КМ. Для оценки истинного количества бластных клеток и исключения раннего рецидива КМ должен быть исследован в фазу аплазии во время проведения интенсивной химиотерапии. К общепринятым критериям ответа МДС и ОМЛ на терапию относятся: <5% бластных клеток в пересчете на количество всех мононуклеаров КМ, присутствие морфологически нормального гемопоэза и возвращение к нормальным значением показателей периферической крови. Кроме того, должна быть подтверждена элиминация инфекционных осложнений, появившихся в период аплазии, связанной с лечением.
После завершения лечения, пациенты должны проходить регулярное клиническое наблюдение с исследованием системы кроветворения. Исследование КМ у пациентов в ремиссии не имеет большого значения и не рекомендуется к регулярному проведению. Клиническое значение молекулярного мониторинга (PCR) ремиссии у пациентов при наличии хромосомных аберраций, позволяющего выявлять ранние молекулярные рецидивы и отслеживать динамику минимальной резидуальной болезни (MDR) не представляется существенным при отсутствии морфологических признаков возврата болезни. Особенно важно отсутствие на данный момент доказательств успеха раннего возобновления терапии у пациентов на фоне сохраняющейся гематологической ремиссии.